I Connettivi a Costituzione Cellulare
I Connettivi a Costituzione Cellulare sono caratterizzati dalla presenza di scarsissima sostanza fondamentale tra le cellule.
I connettivi a costituzione cellulare sono:
- l'endotelio
- il tessuto cordoide
- il tessuto adiposo (bianco e bruno).
Endotelio
[modifica]L'Endotelio o Tessuto Endoteliale è un tipo particolare di tessuto epiteliale pavimentoso non stratificato di derivazione mesenchimale che costituisce il monostrato cellulare che riveste la superficie interna dei vasi sanguigni, dei vasi linfatici e del cuore (endocardio). L'endotelio è l'organo più voluminoso del corpo umano, ha un peso totale di 1,0-1,8 Kg e una superficie stimata di circa 400 m2 (secondo altri autori 1000 m2).
Le cellule che formano l'endotelio sono chiamate cellule endoteliali: cellule endoteliali vascolari, se in contatto con il sangue, e cellule endoteliali linfatiche, se in contatto con la linfa. Le cellule endoteliali vascolari si trovano nell'intero sistema circolatorio, dal cuore alle vene e sono esposte sia al flusso ematico che ai costituenti plasmatici. La loro struttura presenta variazioni (eterogeneità dell'endotelio) a seconda dei diversi compartimenti cui appartengono (arterioso, venoso e capillare). Vi sono notevoli differenze nelle cellule endoteliali che sono deputate a funzioni di filtraggio speciali; esempi di tali strutture possono essere trovate nei glomeruli renali e nella barriera emato-encefalica.
Sulla base del tipo di contatto che si stabilisce tra le cellule endoteliali, l'endotelio viene classificato in continuo, fenestrato e discontinuo. L'endotelio continuo si ritrova nell'endocardio, nell'intima delle arterie e delle vene e in numerosi distretti capillari (cutanei, muscolari, polmonari, cerebrali, spinali e reitinici), mentre gli altri tipi sono esclusivi di alcuni letti capillari: endotelio fenestrato dei capillari renali e glomerulari, delle ghiandole esocrine ed endocrine, dei villi intestinali e dei plessi coroidei; endotelio discontinuo dei sinusoidi epatici, splenici e midollari.
Le cellule endoteliali svolgono molteplici funzioni di primaria importanza per la biologia vascolare e per il mantenimento dell'omeostasi dell'intero organismo. L'endotelio costituisce una barriera anatomica tra il sangue e l'intima dei vasi o lo spazio interstiziale tissutale: si tratta sia di una barriera fisica semipermeabile che di una interfaccia biologica capace di rispondere ai segnali chimici e meccanici generati dai due compartimenti tra i quali l'endotelio è interposto (vedi Patobiologia dell'aterosclerosi: endotelio e stress meccanici). Le sue funzioni comprendono:
- regolazione della permeabilità vasale;
- regolazione del tono e della struttura dei vasi;
- angiogenesi;
- controllo dell'emostasi;
- controllo dell'infiammazione (es. reclutamento dei neutrofili);
- funzioni endocrino-metaboliche (es. metabolismo delle lipoproteine e di alcuni ormoni).
Etimologia
[modifica]Ancora nel 1856, nel grande trattato di Todd e Bowman (The physiological anatomy and physiology of man), il rivestimento interno dei vasi era indicato come "strato epiteliale". Il primo a riconoscere, con il metodo dell'impregnazione argentica, che i capillari non sono dei semplici passaggi membranosi attraverso i tessuti, ma possiedono una parete cellulare propria, è stato Friedrich Daniel von Recklinghausen nel 1860; il termine endotelio (dal greco endo-, interno, e telé, capezzolo, per la somiglianza con il rivestimento interno del capezzolo) fu proposto dallo svizzero Wilhelm His senior (1831-1904) nel 1865, durante le sue ricerche in campo embriologico, per indicare il rivestimento interno dei vasi e delle cavità pleuriche e peritoneali (attuale mesotelio), distinguendolo dall'epitelio che costituisce il rivestimento delle strutture anatomiche a contatto con l'ambiente esterno.
Anatomia microscopica
[modifica]La cellula endoteliale è una cellula pavimentosa mononucleata, di forma poligonale allungata, con prevalenza della morfologia allungata nelle arterie e di quella poligonale nelle vene. La forma allungata, orientata secondo la direzione del flusso sanguigno domina dove il flusso è rapido, unidirezionale e laminare, mentre è meno evidente nei tratti a flusso lento e disturbato. Lo spessore medio delle cellule endoteliali varia da 0,1-0,2 μ nei capillari e nelle vene a 1 μ nell'aorta ed è massima a livello del nucleo (2-3 μ); la lunghezza si aggira intorno ai 30-50 μ e la larghezza ai 10-20 μ. Il nucleo è ovoidale e allungato e il citoplasma contiene, oltre ai consueti organelli (Golgi, mitocondri, reticolo endoplasmatico, ribosomi, lisosomi e citoscheletro), numerose vescicole (particolarmente abbondanti nei capillari, dove costituiscono circa il 20% del volume cellulare) e i Corpi di Weibel-Palade (WPB). Le cellule endoteliali sono cellule polarizzate, in quanto la superficie luminale è differente da quella abluminale (basale).
Vescicole. Sono presenti sia vescicole rivestite da clatrina sia vescicole non rivestite contenenti caveolina e cavina. Le prime intervengono nell'endocitosi, svolgendo la funzione di trasporto intracellulare, dalla membrana plasmatica agli endosomi o all'apparato di Golgi, come nel caso dell'endocitosi recettore-mediata della transferrina e delle lipoproteine a bassa densità (LDL). Le seconde sono molto più numerose, hanno un diametro di 50–70 nm e sono responsabili del trasporto di sostanze attraverso la cellula endoteliale (transcitosi); sono particolarmente numerose nei capillari non fenestrati: la loro densità varia da 200/μm3 nelle arteriole a 600/μm3 nelle venule postcapillari, per raggiungere 900-1200/μm3 nei capillari, ad eccezione di alcuni letti capillari, come quelli polmonari (130/μm3) e soprattutto la barriera emato-encefalica (<100/μm3). Mentre l'endocitosi assolve al compito di fornire alla cellule sostanze destinate al proprio metabolismo, la transcitosi interviene nel trasferimento di composti destinati all'ambiente extracellulare.
Corpi di Weibel-Palade. I WPB sono vescicole secretorie, specifiche delle cellule endoteliali, che al microscopio elettronico appaiono allungate (rod-shaped), con dimensioni di circa 0.2 x 2 μ, elettrondense e di aspetto regolarmente striato per la presenza di strutture tubulari parallele, costituite dai polimeri del Fattore di von Willebrand (VWF). Oltre a VWF, i corpi WPB contengono la proteina adesiva P-selectina.
Le principali differenze morfologiche tra endotelio arterioso e venoso riguardano soprattutto: spessore cellulare (minore nelle vene, ad eccezione delle HEV o venule post-capillari a endotelio alto dei linfonodi); sviluppo degli apparati giunzionali (molto meno serrati nelle vene, in modo particolare nelle venule post-capillari); abbondanza delle vescicole citoplasmatiche (presenza dei vesiculo-vacuolar organelles o VVO nelle venule post-capillari). Tali differenze strutturali sono in relazione con la permeabilità e con i parametri emodinamici (lo stress da attrito o shear stress è di 1–5 dynes/cm2 nel settore venoso e di 10–40 dynes/cm2 in quello arterioso) (Vedi Patobiologia dell'aterosclerosi - Stress emodinamici).
Superficie cellulare
[modifica]La superficie luminale presenta numerose fossette a forma di fiasco, dette caveole (lett. piccole caverne), ed è "rivestita" dal glicocalice e dallo strato endoteliale superficiale (ESL, endothelial superficial layer). Le caveole, invaginandosi, danno origine alle vescicole contenenti caveolina. Il glicocalice è uno strato glicoproteico con spessore variabile a seconda dello stato funzionale della cellula (in media misura circa 60-110 nm). Questo rivestimento è ricco di cariche negative ed è formato da glicoproteine (es. molecole di adesione, molecole del sistema emostatico), eparansolfato-proteoglicani (es. sindecano, glipicano) e glicolipidi di membrana: la componente glucidica di queste molecole sporge dalla superficie della membrana cellulare (vedi Patobiologia dell'aterosclerosi - Proteoglicani). Al glicocalice luminale aderiscono molecole plasmatiche che formano uno strato spesso (500-1000 nm) che ricopre il glicocalice e che viene indicato come ESL. Sia il glicocalice che l'ESL hanno una notevole importanza funzionale: agiscono da filtro molecolare (influenzando la permeabilità), modulano lo shear stress e inibiscono l'adesione di leucociti e di piastrine. Nei piccoli vasi e nei capillari la presenza di questo strato aumenta le resistenze al flusso e respinge i globuli rossi, tanto che nei capillari l'ematocrito ha valori più bassi rispetto ai valori sistemici. Durante i processi infiammatori il glicocalice viene represso, contribuendo all'adesione dei leucociti all'endotelio.
La superficie basale possiede anch'essa numerose caveole ed è fermamente ancorata alla membrana basale (vedi intima). Tale ancoraggio è opera dl due classi di proteine che mediano l'adesione cellula-matrice extracellulare (ECM): le integrine e i suddetti eparansolfato-proteoglicani; quasi tutte le proteine che compongono la ECM possiedono siti di legame per entrambe queste due classi. Le integrine e i sindecani presentano un dominio extracellulare (che si lega all'ECM), un dominio transmembranaceo (che attraversa la membrana cellulare) e un dominio intracellulare (che interagisce con il citoscheletro). In tal modo queste proteine adesive si comportano anche da meccanocettori: rispondono alla deformazione e trasmettono segnali dall'ambiente extracellulare all'interno della cellula. Esse possono essere organizzate in complessi strutturali plurimolecolari, chiamati "adesioni focali". Le adesioni focali appaiono come piccole regioni elettrondense della membrana, di forma allungata, con il diametro maggiore di pochi micron, strettamente aderenti alla ECM e direttamente connesse al citoscheletro. La loro impalcatura portante è costituita dalle integrine, ma alla loro formazione partecipano oltre un centinaio di proteine diverse, sindecani inclusi. Le adesioni focali sono complessi dinamici, che vengono assemblate e disassemblate a seconda delle necessità funzionali.
Citoscheletro
[modifica]Il citoscheletro è formato dai filamenti di actina e dalle proteine associate (miosina, vinculina, ecc.). Al microscopio elettronico, il citoscheletro appare organizzato in tre sistemi fondamentali: una rete periferica di filamenti posti subito al di sotto della membrana plasmatica; un addensamento sub-membranoso di microfilamenti in corrispondenza della superficie basale e delle giunzioni intercellulari; fibre dello stress (fasci di microfilamenti) connessi sia con le adesioni focali della membrana plasmatica basale sia con la membrana apicale. Il citoscheletro è importante per mantenere la morfologia della cellula, per stabilizzare l'integrità delle strutture di adesione e per modulare la permeabilità endoteliale. La riorganizzazione del citoscheletro in risposta agli stress emodinamici si accompagna a modificazioni della forma cellulare. L'esposizione a uno shear stress elevato induce un maggior sviluppo delle fibre dello stress, uno sviluppo minore della rete periferica di filamenti e un allungamento della forma cellulare; lo shear stress basso ha un effetto opposto sull'organizzazione dei microfilamenti e determina l'assunzione della forma poligonale.
Cilia primarie
[modifica]In alcune condizioni particolari sono state descritte sulla superficie endoteliale cilia primarie solitarie (cilia immobili). Le cilia primarie hanno una lunghezza di 1-5 μ e sono caratterizzate da una struttura interna (assonema) formata solo da una corona periferica di nove coppie di microtubuli, senza la coppia centrale di microtubuli (struttura "9+0") che distingue le più comuni cilia mobili (struttura "9+2"). Esse svolgono una funzione meccanorecettoriale: sono capaci di rispondere a forze emodinamiche estremamente basse (0.007 dyne/cm2) e trasmettono segnali chimici (es. Ca+2) e meccanici all'interno della cellula. Alla genesi dei primi concorrono le proteine di membrana policistina 1 e 2 e poliductina/fibrocistina (proteina legata allo sviluppo del rene policistico). I segnali meccanici sono invece trasmessi dai microtubuli dell'assonema al citoscheletro citoplasmatico. Le cilia primarie rispondono anche a forze meccaniche generate nella matrice extracellulare (ECM) grazie alla connessione tra le adesioni focali e il citoscheletro. Si ritiene che le cilia primarie siano espresse solo in presenza di uno shear stress particolarmente basso ed è stato ipotizzato che esse possano intervenire nello sviluppo dell'aterosclerosi.
Giunzioni intercellulari
[modifica]Nell'endotelio continuo, le cellule endoteliali sono separate da stretti spazi intercellulari di circa 15-20 nm di ampiezza, occupati da glicosaminoglicani (lo storico "cemento" intercellulare). Tra le cellule endoteliali contigue si stabiliscono anche zone circoscritte di contatto più ravvicinato, dove le cellule aderiscono intimamente tra loro, creando così una barriera anatomica dinamica che limita la diffusione delle molecole plasmatiche. Le strutture macromolecolari responsabili di tale intima adesione sono indicate come "complessi giunzionali" (giunzioni cellulari), distinti in: giunzioni aderenti (adherens junctions), giunzioni occludenti (tight junctions) e giunzioni comunicanti (gap junctions). Le tight junctions sono più numerose nel settore arterioso della circolazione (particolarmente sviluppate nell'endotelio delle grandi arterie); nei capillari il massimo sviluppo si osserva nel sistema nervoso centrale (barriera emato-encefalica); nelle venule post-capillari sono assenti. Le gap junctions permettono la comunicazione intercitoplasmatica tra cellule endoteliali attraverso il passaggio di piccoli soluti (p.m. <1000-1500 daltons), come ioni, metaboliti e secondi messaggeri; sono composte dalle connessine Cx37, Cx40 e Cx43 che fomano canali (connessoni) nella membrana. La connessina 43 (Cx43) sembra prevalere nelle sedi di flusso disturbato.
Le giunzioni mio-endoteliali (MEJ) sono estroflessioni della membrana plasmatica basale che, spingendosi attraverso discontinuità della lamina elastica interna, mettono in comunicazione diretta le cellule endoteliali con le cellule muscolari lisce della tonaca media, consentendo una puntuale coordinazione funzionale tra queste cellule. Proprio per questo le MEJ sono più numerose nelle piccole arterie di resistenza (dove la regolazione endoteliale del tono vasale riveste un'importanza maggiore) rispetto alle grandi arterie di conduzione. Nelle MEJ sono presenti gap junctions che permettono l'accoppiamento elettro-chimico tra endotelio e muscolatura vasale.
Fisiologia
[modifica]L'endotelio è un organo endocrino, paracrino e autocrino in grado di liberare una gran varietà di sostanze nel sangue e nello spazio interstiziale, le quali possono agire a distanza (attività endocrina), sulle cellule vicine (attività paracrina) o sulla stessa cellula che le ha prodotte (attività autocrina). Le sostanze prodotte dall'endotelio comprendono composti vasoattivi, fattori di crescita, mediatori dell'infiammazione (citochine, chemochine), molecole di adesione, molecole della sostanza extracellulare, proteine del sistema emostatico, enzimi. Attraverso questa ampia gamma di composti l'endotelio interviene nel controllo dell'omeostasi vasale, dell'infiammazione, dell'immunità, dell'emostasi e svolge una serie di importanti funzioni metaboliche. Una delle dimostrazioni più eclatanti dell'importanza dell'endotelio si ricava dal fatto che l'applicazione dell'acetilcolina alla superficie intimale integra causa dilatazione del vaso, mentre dopo rimozione dell'endotelio l'applicazione provoca vasocostrizione. Questo apparente paradosso ha la sua spiegazione nel fatto che la vasodilatazione è determinata dall'azione dell'acetilcolina sull'endotelio, mentre la vasocostrizione è dovuta alla stimolazione diretta delle cellule muscolari lisce.
L'attività secretoria dell'endotelio è sia costitutiva (basale) che inducibile in risposta ai vari stimoli: per la sua posizione di interfaccia tra sangue e parete vasale/tessuto, l'endotelio è in grado di rispondere ai cambiamenti del flusso, alle molecole plasmatiche, alle cellule ematiche e agli stimoli provenienti dall'ambiente subendoteliale.
Per la fisiopatologia dell'endotelio vediDisfunzione endoteliale.
Permeabilità
[modifica]L'endotelio continuo si comporta da barriera semipermeabile: limita il passaggio delle cellule ematiche e delle proteine plasmatiche, ma si lascia attraversare dai soluti di piccole dimensioni, verso i quali la permeabilità varia in base sia alla solubilità delle molecole nei grassi e nell’acqua sia alla loro grandezza (raggio molecolare, Mr). Con l’eccezione della barriera emato-encefalica, gli endoteli continui non fenestrati sono liberamente permeabili all’acqua, ai soluti liposolubili e ai composti idrosolubili di piccole dimensioni, mentre sono attraversati con difficoltà dalle macromolecole.
Gli endoteli continui si comportano come se possedessero due tipi di pori funzionali (teoria dei due pori): “piccoli pori” di diametro di circa 8-10 nm (secondo Guyton il diametro è di 6-7 nm) che consentono il passaggio esclusivamente ai soluti di Mr <3 nm e “grandi pori” di diametro di circa 40-60 nm per il passaggio delle macromolecole di Mr >3.6 nm. Nei capillari dei muscoli scheletrici il rapporto numerico tra piccoli e grandi “pori” è di circa 4000:1. Gli studi di microscopia elettronica hanno indicato, come equivalenti morfologici dei "piccoli pori funzionali", gli spazi intercellulari con i loro apparati giunzionali, mentre le caveole/vescicole non rivestite e i canali intracellulari (tubular-vesicular channels), formati dalla sequenza di vescicole comunicanti tra loro, corrisponderebbero ai “grandi pori”.
Sulla base di queste evidenze si ritiene che il passaggio di acqua e di soluti attraverso l’endotelio avvenga lungo due vie: attraverso gli spazi (fessure) intercellulari (via paracellulare) o attraverso le cellule endoteliali stesse (via transcellulare). L'acqua (p.m. 18 e Mr 0.12 nm) per il 60% filtra per via paracellulare, ma per il restante 40% utilizza la via transcellulare, servendosi però della via specifica costituita dalle proteine di membrana acquaporine.
Le sostanze liposolubili, come ossigeno e anidride carbonica, sono in grado di attraversare direttamente la membrana plasmatica, per cui il loro passaggio avviene molto rapidamente per diffusione attraverso le cellule endoteliali.
Le molecole idrosolubili di piccole dimensioni, con p.m. <40.000 daltons e Mr <3 nm, come acqua, monosaccaridi (glucosio, mannitolo, fruttosio), aminoacidi, urea e piccole proteine (mioglobina: p.m. 17.600 e Mr 2 nm), passano facilmente lungo la via paracellulare; la loro diffusione avviene velocemente, sebbene le fessure interendoteliali costituiscano soltanto 1/1000 dell’intera superficie endoteliale.
Le macromolecole di p.m. >60.000 e Mr >3.6 nm (emoglobina p.m. 68.000 e Mr 3,2 nm; albumina p.m. 69.000 e Mr 3.6 nm; HDL p.m. 180.000-360.000 e Mr medio 4.5 nm; IgM p.m. 950.000 e Mr 11.5 nm; LDL in media p.m. 2.300.000 e Mr 9-13 nm) in condizioni fisiologiche sono trasportate attivamente (con dispendio di energia) per la via transcellulare costituita dalle vescicole citoplasmatiche (transcitosi). Per quanto riguarda l’insulina (p.m. 6000) dai lavori finora pubblicati risulta che le cellule endoteliali aortiche trasportano l’ormone con un processo recettore-dipendente coinvolgente le caveole, mentre l’endotelio della microcircolazione utilizza le vescicole rivestite da clatrina. Poiché le vescicole responsabili della transcitosi hanno un diametro intorno ai 100 nm, le molecole di dimensioni particolarmente grandi (Mr >35-40 nm) non possono attraversare gli endoteli continui. Tale situazione si verifica per le lipoproteine più voluminose (chilomicroni e lipoproteine a densità molto bassa o VLDL), mentre il prodotto del loro metabolismo, cioè le lipoproteine a densità intermedia (IDL, Mr 25-35 nm), mantengono la capacità di oltrepassare la barriera endoteliale (vedi Lipoproteina). Ciò spiega perché l'iperchilomicronemia non rappresenti una condizione a rischio aterosclerosi.
In particolare, per le LDL esisterebbero due modalità di trasporto: quella clatrina-mediata, che capta le LDL per le necessità metaboliche della cellula, e quella caveolina-dipendente, che le trasporta nello spazio subendoteliale: l'endocitosi clatrina-mediata utilizza il recettore per le LDL naturali (LDLR) ed è regolata dal fabbisogno cellulare di colesterolo; la transcitosi delle LDL da parte delle caveole è invece indipendente dal fabbisogno cellulare e può essere recettore-indipendente (endocitosi in fase fluida o pinocitosi) o dipendente dallo scavenger-receptor SR-B1, che è in grado di legare sia le LDL modificate che quelle naturali. Secondo alcuni la transcitosi delle lipoproteine potrebbe avvenire anche tramite le vescicole rivestite da clatrina. Predrescu ha identificato un ulteriore sistema di trasferimento delle LDL che coinvolge l'esocitosi mediata dal recettore SNAP (SNARE).
Grazie alla sua semipermeabilità, l'endotelio controlla la quantità e la composizione del liquido interstiziale presente nei tessuti, parete vasale compresa. Poiché il liquido interstiziale è il mezzo fisico che mette in comunicazione il sangue con le cellule, la permeabilità dell'endotelio svolge una funzione vitale per l'organismo, consentendo da una parte l'ingresso nei tessuti di ormoni e metaboliti e, dall'altra, la rimozione dei prodotti del catabolismo. La permeabilità è una funzione dinamica che viene modulata a seconda delle necessità fisiologiche e delle condizioni patologiche, come nel caso delle reazioni infiammatorie, nelle quali la permeabilità endoteliale aumenta enormemente. Infatti i mediatori dell’infiammazione, legandosi ai propri recettori, causano il riarrangiamento delle giunzioni intercellulari, cosicché le macromolecole possono facilmente attraversare l’endotelio per la via paracellulare. Anche nei tumori i capillari e le venule sono iperpermeabili alle macromolecole a causa della secrezione di citochine tumorali (es. vascular endothelial growth factor o VEGF).
Particolare importanza ha il passaggio dell’albumina. Poiché l’albumina è la più abbondante proteina plasmatica, la sua corretta filtrazione è essenziale per il mantenimento della pressione colloido-osmotica dello spazio extravasale (circa il 60% dell’albumina totale si trova nello spazio interstiziale). Il suo attraversamento della barriera endoteliale avviene per transcitosi recettore-dipendente: la glicoproteina gp60 o albondina (albumin-binding protein) presente nelle caveole. Dal momento che l’albumina plasmatica è il veicolo per il trasporto nel sangue di numerose sostanze insolubili in acqua, con la transcitosi dell’albumina vengono trasportati anche composti come vitamine liposolubili, acidi grassi a catena lunga e ormoni steroidei.
Per le forze fisiche che determinano il movimento di acqua e soluti attraverso l'endotelio dei capillari vedi Scambi capillari e Equazione di Starling.
Via Transcellulare
[modifica]Le macromolecole attraversano l'endotelio per transcitosi, processo che è mediato dal sistema delle caveole-vescicole non rivestite e dal sistema vescicolo-vacuolare VVO (vesiculo-vascuolar organelles).
Come descritto in Anatomia microscopica, le caveole sono invaginazioni della membrana plasmatica ("fossette") di circa 50-100 nm di diametro. La membrana delle caveole contiene caveolina-1 e cavina ed è ricca di colesterolo. Gli orifici (stomi) delle caveole sono di solito chiusi da sottili diaframmi di 6-8 nm di spessore, contenenti la proteina PV1 (plasmalemmal vesicle protein-1). Oltre alla funzione di trasporto transcellulare, le caveole hanno grande importanza nel metabolismo del colesterolo, nella generazione di segnali intracellulari (es. in risposta allo shear stress e a VEGF) e nella sintesi dell'ossido di azoto (NO).
Sebbene le caveole siano ritenute il più importante sistema di trasporto per le macromolecule, nelle venule post-capillari sono presenti grappoli di centinaia di grandi vescicole caveolina-1 positive di diametro variabile da 80 nm a 140 nm che sono indicati come VVO. Come nel caso delle caveole, le vescicole del VVO sono collegate sia le une alle altre sia alla membrana plasmatica tramite orifici che possono essere aperti o chiusi da diaframmi. È opinione diffusa che il VVO sia costituito dalla fusione delle caveole. Il VVO attraversa completamente il citoplasma della cellula endoteliale dalla superficie luminale a quella basale, formando canali transcellulari, ma può aprirsi anche nelle fessure intercellulari.
Via Paracellulare
[modifica]La via paracellulare coinvolge le fessure interendoteliali: questi spazi hanno un'ampiezza di circa 15-20 nm e una lunghezza di 0,15-1,5 mm e sono attraversati, e ristretti, dalle giunzioni occludenti (tight junctions), in corrispondenza delle quali lo spazio intercellulare si riduce a soli 4 nm di diametro. Tuttavia, con eccezione della barriera emato-encefalica, le giunzioni occludenti delle cellule endoteliali non formano una fascia continua, lungo tutto il contorno della cellula (come negli epiteli), ma sono organizzate in segmenti discontinui e non allineati, disposti cioè ad altezze diverse sulla parete laterale delle cellule endoteliali. Da questa disposizione risulta che le discontinuità formerebbero dei percorsi tortuosi e troppo ampi per costituire un filtro efficace alla diffusione dei soluti. In una ricostruzione tridimensionale, alle discontinuità è stata attribuita un’ampiezza di circa 22 nm e una lunghezza di 40-90 nm. La funzione di filtro poroso sarebbe quindi svolta dalle glicoproteine di membrana che occupano le fessure interendoteliali ("teoria della matrice di fibre" di Curry e Michel). Pertanto la barriera alla diffusione viene attualmente identificata nel glicocalice che riveste sia la superficie endoteliale che le fessure intercellulari (“modello glicocalice-fessure"): la porosità del glicocalice rappresenterebbe così i “piccoli pori” dei fisiologi. Ciò permette di spiegare perché la rimozione delle proteine o della sola albumina (che partecipa alla formazione dello strato endoteliale superficiale, ESL) dall'ambiente aumenta la permeabilità della barriera endoteliale.
Controllo del tono vasale
[modifica]Il tono vasale è controllato a livello sistemico e/o locale dal sistema nervoso autonomo, da ormoni, da sostanze vasoattive plasmatiche e tissutali e da mediatori prodotti dall’endotelio. L’endotelio svolge un ruolo fondamentale nel controllo della funzionalità delle arterie, delle vene e del microcircolo. La secrezione endoteliale è modulata dalle forze emodinamiche e da una varietà di segnali chimici. Le cellule endoteliali possiedono, infatti, un complesso apparato recettoriale in grado di essere attivato dalle variazioni di flusso (shear stress) e da un ampio spettro di sostanze (ormoni, mediatori dell’infiammazione, endotossine batteriche, LDL ossidate, ecc.). Il controllo della muscolatura vasale viene esercitato dall'endotelio attraverso tre modalità: attività enzimatica su substrati plasmatici (es. enzima convertitore dell'angiotensina); secrezione paracrina (locale) di mediatori vasoattivi; accoppiamenti diretti con le cellule muscolari lisce tramite le MEJ.
In generale, i mediatori vasodilatatori possiedono anche azione anti-proliferativa, anti-trombotica e anti-aterogena, mentre le sostanze vasocostrittrici hanno azioni opposte. In condizioni fisiologiche prevale la produzione di sostanze vasodilatatrici. La produzione dei composti vasoattivi endoteliali varia con l'età e con le condizionioni patologiche, nelle quali l'eccessiva produzione di radicali liberi sposta l'equilibrio verso la prevalenza delle sostanze vasocostrittrici/pro-aggreganti piastriniche.
Sulla base della natura chimica i mediatori vasoattivi endoteliali possono essere classificati in: composti lipidici (eicosanoidi; fattore attivante le piastrine, PAF), peptidi (endotelina-1, ET-1; angiotensina II, ATII; fattore di crescita di derivazione piastrinica, PDGF; peptide natriuretico, NP), di-nucleotidi (uridin-adenosin-tetrafosfato, UP4A), composti inorganici (ossido di azoto, NO; radicali liberi dell'ossigeno, ROS; acido sulfidrico, H2S; ioni K+).
Dalla ossidazione dell'aminoacido L-arginina in L-citrullina, ad opera delle nitrossido-sintetasi (NOS), deriva l'ossido nitrico (NO). Questo mediatore attiva, nelle cellule muscolari lisce, l'enzima guanil-ciclasi che genera il secondo messaggero GMPc, in grado di indurre rilasciamento della muscolatura. NO è prodotto costitutivamente dalla nitrossido-sintetasi endoteliale (eNOS); nell'endotelio è presente anche la nitrossido-sintetasi inducibile (iNOS).
Derivati dell'acido arachidonico. L'acido arachidonico (acido grasso polinsaturo a 20 atomi di carbonio, C20:4), liberato dai glicerofosfolipidi di membrana per azione della fosfolipasi A2, è una delle più importanti fonti di metaboliti vasoattivi. Da esso derivano numerosi eicosanoidi (dal greco eikosi, venti, e eidos, forma): prostanoidi, leucotrieni e lipossine, che sono ormoni locali (o autacoidi, dal greco autòs, se stesso, e àkos, rimedio). Questo acido grasso può infatti essere metabolizzato dalle ciclossigenasi (COX1 e 2), dalle lipossigenasi (LOX) e dalla epossigenasi (citocromo P450 monossigenasi, CYP450).
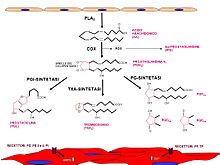
Dalle COX endoteliali derivano sei prostanoidi, ovvero prostaglandine (PG) e trombossano (Tx): PGI2 (prostaciclina) e PGD2 con attività vasodilatatoria e anti-aggregante piastrinica; PGH2, PGF2α e TxA2 ad azione vasocostrittrice e pro-aggregante; PGE2 ad azione variabile a seconda della concentrazione e del letto vasale. Questi mediatori esercitano le loro azioni interagendo con i recettori di membrana DP, EP, FP, IP e TP (recettore TxA2) accoppiati alle proteine G: DP, EP2, EP4 e IP aumentano l'AMP ciclico (AMPc) mediante le proteine Gs; TP, EP1 e FP innalzano il calcio intracellulare per mezzo delle Gq; EP3 riduce la concentrazione di AMPc attraverso le Gi. Per la loro capacità di ossidare substrati, le COX sono anche fonte di radicali liberi dell'ossigeno (anioni superossido, O2-).
Dall'epossigenasi derivano gli acidi epossi-eicosa-trienoici (EET) e di-idrossi-eicosatrienoici (DHET) ad azione vasodilatatrice; azione analoga hanno gli acidi idrossi-eicosa-tetraenoici (HETE) derivati dalla 15-lipossigenasi endoteliale (15-LOX-1). HETE e EET attivano i canali del K+ calcio-dipendenti delle cellule muscolari lisce, provocando iperpolarizzazione della muscolatura e rilasciamento vasale.
Mediatori vasodilatatori
[modifica]
In condizioni fisiologiche prevale la liberazione endoteliale di mediatori vasodilatatori: NO (ossido nitrico), PGI2 (prostaciclina) e EDHF (endothelium-derived hyperpolarization factor ). Il loro ruolo è stato dimostrato negli uomini e negli animali in vivo ed ex vivo in arterie isolate, sia in condizioni basali che dopo stimolazione con agonisti (es. acetilcolina, bradichinina) o esposizione al flusso. La vasodilatazione endotelio-dipendente indotta dai diversi agonisti varia a seconda della specie animale: l'acetilcolina causa rilasciamento endotelio-dipendente delle arterie sistemiche di tutte le specie esaminate (variazioni si hanno però nel comportamento delle arterie polmonari e cerebrali e delle vene) (nota 1); la bradichinina provoca rilasciamento delle arterie umane e canine, ma non di quelle di coniglio né di gatto; l'istamina determina vasodilatazione delle arterie di ratto, ma non di coniglio.
L’aumento delle resistenze vasali totali e della pressione arteriosa media che si ottiene, in soggetti sani, dalla somministrazione di inibitori delle COX (es. indometacina), delle NOS (es. L-NMMA) e di EDHF (es. KCl) è a favore di un ruolo fisiologico di NO, PG e EDHF nel controllo del tono vasale. La produzione di questi composti è stimolata dallo shear stress e da numerosi agonisti ed è regolata in modo tale che il deficit di uno di essi venga compensato dall'iperproduzione degli altri.
EDHF è costituito da un insieme di sostanze capaci di provocare iperpolarizzazione delle cellule muscolari lisce. EDHF viene infatti definito come "il complesso di sostanze che causano la vasodilatazione che residua dopo somministrazione di inibitori di NOS e di COX e che è inibita dai bloccanti dei canali del K+ o dalle alte concentrazioni extracellulari di K+". EDHF probabilmente include derivati dell'acido arachidonico, peptidi, CO (monossido di carbonio), H2S (acido sulfidrico) e H2O2.
Un'altra via attraverso la quale le cellule endoteliali possono causare iperpolarizzazione della muscolatura vasale è quella delle giunzioni MEJ; in questo caso è il passaggio di ioni K+ direttamente dall'endotelio alla tonaca muscolare che causa iperpolarizzazione: l'iperpolarizzazione riduce l'ingresso di calcio (Ca++) nelle cellule muscolari lisce attraverso i canali Ca-voltaggio dipendenti e determina vasodilatazione.
Una serie di lavori nell’uomo e negli animali hanno dimostrato che l’importanza dei singoli mediatori muta con il variare del calibro dei vasi: la vasodilatazione delle arterie elastiche e muscolari dipende principalmente da NO, mentre quella arteriolare è influenzata maggiormente da EDHF e PGI2.
1) Ossido Nitrico (NO)
[modifica]
L'intervento di NO nel tono vasale basale nell'uomo è dimostrato dalla constatazione che l'inibizione della sintesi di NO con analoghi dell'arginina provoca un aumento della pressione arteriosa, aumento che viene annullato dalla somministrazione di L-arginina. In uno studio in soggetti sani normotesi, l'inibitore della NOS N-monometil-L-arginina (L-NMMA) ha determinato un aumento della pressione arteriosa media di 8-15 mmHg, mentre con l'inibitore N-nitro-L-arginina-metil-estere (L-NAME) l'aumento è stato di 10-23 mmHg; all'effetto tardivo sulla pressione arteriosa sembra partecipare l'attivazione simpatica dovuta all'inibizione della NOS del sistema nervoso centrale (nNOS). Allo stesso modo i ratti con deficit genetico di NOS endoteliale (eNOS -/-) sono ipertesi. La sintesi di NO declina con l'età. La compromissione della sintesi di NO nella disfunzione endoteliale è responsabile di un eccesso di vasocostrizione con un aumento del tono vasale, nonché di una diminuzione dell'attività anti-aggregante. In presenza di stress ossidativi, gli O2- interagiscono con NO inattivandolo e formando perossinitrito (ONOO−) che è a sua volta un radicale libero dell'azoto (RNS).
2) Prostaciclina (PGI2)
[modifica]Il principale mediatore vasodilatatore derivato dalle COX nelle cellule endoteliali umane è la prostaglandina bicilcica PGI2 (prostaciclina). La somministrazione di inibitori delle COX (indometacina) in volontari sani ha provocato un aumento delle resistenze vasali totali (+20%) e della pressione arteriosa media (+10 mmHg), mentre l'infusione di acido acetilsalicilico nell'arteria brachiale ha determinato una riduzione del 32% del flusso sanguigno dell'avambraccio. L'infusione di PGI2 negli animali anestetizzati (cane, ratto, coniglio) causa ipotensione, sia che la somministrazione venga fatta per via endovenosa che endoarteriosa, poiché la PGI2, a differenza delle altre prostaglandine, non viene metabolizzata nel polmone; la sua perfusione in cuori isolati induce dilatazione delle arterie coronarie. La PGI2 è la più abbondante prostaglandina prodotta dall'endotelio: la sua concentrazione è 10-100 superiore a quella delle altre prostaglandine endoteliali, ma declina con l'età. Si tratta di una delle più potenti sostanze vasodilatatrici dell'organismo, con un effetto circa 8 volte maggiore della PGE2, tanto che la prostaciclina sintetica (epoprostenol) e i suoi analoghi (iloprost e treprostinil) sono impiegati per il trattamento dell'ipertensione polmonare. Sebbene la PGI2 a concentrazioni fisiologiche abbia azione vasodilatatrice, ad alte concentrazioni essa acquista modeste proprietà vasocostrittrici; il diverso comportamento è in relazione ai differenti recettori muscolari attivati: IP nel primo caso, TP nel secondo. La stimolazione del recettore IP causa l'attivazione della proteina Gs e l'aumento di AMPc nelle cellule muscolari lisce, con conseguente apertura dei canali K+ ATP-dipendenti e iperpolarizzazione. La delezione del gene IP nei topi si accompagna a ipertensione e diminuzione dell'attività antiaggregante; al contrario, i topi con deficit genetico del recettore TP sono normotesi, ma hanno tendenza al sanguinamento.
La PGI2 è sintetizzata all'azione sequenziale delle COX e della prostaciclina-sintetasi (PGIS). Sia la COX1 che la COX2 sono espresse nell'endotelio: la COX1 (COX costitutiva) è espressa costitutivamente ed è prevalente in condizioni basali; l'espressione della COX2 (COX inducibile) è incrementata da shear stress, citochine infiammatorie, mediatori piastrinici, endotossine batteriche, LDL ossidate, trombina e ipossia. Sebbene gli studi farmacologici con inibitori della COX2 (Coxib) e gli studi sperimentali su topi con deficit del gene Cox2 lascino supporre che la produzione endoteliale di PGI2 sia dovuta principalmente all'attività della COX2, rimangono dubbi su quale sia la COX maggiormente responsabile della formazione della PGI2. La PGIS è estremamente sensibile all'inattivazione da parte del perossinitrito: situazioni di stress ossidativo determinano la deviazione della sintesi dei prostanoidi verso composti vasocostrittori/pro-aggreganti; contemporaneamente i radicali liberi aumentano la stabilità e il numero dei recettori TP. In queste situazioni, l'induzione della COX2 tenta di compensare il deficit di PGI2.
Mediatori vasocostrittori
[modifica]Gli studi sperimentali su preparati animali hanno osservato che, in condizioni fisiologiche, alcuni vasi (es. arterie e vene polmonari) rispondono alla stimolazione con agonisti (es. acetilcolina, acido arachidonico) con la sintesi si sostanze vasocostrittrici e che la vasocostrizione è inibita dalla rimozione dell'endotelio. Nell'uomo i mediatori vasocostrittori hanno importanza soprattutto nell'invecchiamento e in condizioni patologiche (es. ipertensione, diabete) (vedi Trombossani - Fisiopatologia). Nelle indagini sperimentali i mediatori responsabili della vasocostrizione variano in base alla specie animale, al tipo di distretto vasale esaminato e allo stimolo utilizzato. Sono però frequentemente in causa prodotti delle COX, poiché la vasocostrizione viene molto spesso attenuata o prevenuta dagli inibitori dalle COX (es. indometacina).
Le principali sostanze vasocostrittrici comprendono: prostanoidi (TXA2 e PGH2) e altri derivati fosfolipidici (fattore attivante le piastrine, PAF; isoprostani, iPG), peptidi (endotelina 1, ET-1; angiotensina II, ATII; fattore di crescita derivato dalle piastrine, PDGF), ROS (O-2 e H2O2) e di-nucleotidi (uridin-adenosin-tetrafosfato, UP4A). Sebbene gli endoperossidi ciclici (PGH2) siano composti instabili a breve emivita, essi tuttavia possono attivare il recettore TP e provocare vasocostrizione. ATII agisce sia come ormone sistemico che come autacoide locale. Gli isoprostani sono isomeri delle prostaglandine generati dalla perossidazione non enzimatica degli acidi grassi polinsaturi (es. acido arachidonico) presenti nei fosfolipidi di membrana. I ROS si formano durante la sintesi di PGH2 da parte delle COX, nonché per azione di altri enzimi cellulari (es. NOS, NADPH ossidasi, xantina ossidasi); una volta prodotti, essi, e in particolare H2O2, sono in grado di indurre contrazione della muscolatura liscia vasale per azione diretta e indiretta (disattivazione di NO e stimolazione della sintesi di prostanoidi vasocostrittori).
Funzioni emostatiche
[modifica]Le cellule endoteliali intervengono nella regolazione dell'emostasi, producendo, a seconda delle circostanze, attivatori o inibitori delle piastrine, della coagulazione e della fibrinolisi. In condizioni fisiologiche l'endotelio assicura ai vasi un rivestimento non trombogeno che impedisce sia l'attivazione delle piastrine che delle proteine del sistema della coagulazione. La presenza di endotelio evita, inoltre, il contatto del sangue con le fibre collagene e la matrice subendoteliale, in particolare con il fattore di Von Willebrand (vWF) e con il fattore tissutale (TF), una glicoproteina espressa sulle cellule della parete vasale. Le fibre collagene e vWF provocano aggregazione piastrinica, mentre l'interazione di TF con il fattore plasmatico VII forma un complesso che attiva la via estrinseca della coagulazione.
Proteine anti-trombogene sono esposte sulla membrana delle cellule endoteliali (trombomodulina, inibitore della via del fattore tissutale o TFPI, eparansolfato-proteoglicani e CD39) e sostanze solubili sono liberate dall'endotelio (NO, PGI2, proteina C, proteina S, attivatore tissutale del plasminogeno o tPA e urochinasi o u-PA). La trombomodulina, il TFPI, gli eparansolfati-proteoglicani e la proteina C inibiscono la cascata della coagulazione, mentre NO, PGI2 e CD39 possiedono azione antiaggregante piastrinica. NO e PGI2 hanno un'azione antiaggregante diretta; CD39/ENTPD1 (CD39/ecto-nucleoside triphosphate diphosphohydrolase 1) è una ADPasi che degrada l'ADP, uno dei principali attivatori delle piastrine. La trombomodulina si lega alla trombina neutralizzandola e, in più, il complesso trombomodulina-trombina attiva la proteina C. La proteina C attivata si lega alla proteina S e il complesso neoformato acquista proprietà anticoagulanti. L'eparansolfato attiva l'antitrombina III che inibisce la trombina e altri fattori della coagulazione. Sia t-PA che u-PA convertono il plasminogeno in plasmina, enzima capace di degradare la fibrina del coagulo.
Al contrario l'attivazione delle cellule endoteliali si accompagna all'acquisizione di proprietà protrombotiche, come la secrezione del vWF multimerico contenuto nei corpi WP, l'esposizione del TF e la produzione dell'inibitore dell'attivatore del plasminogeno (PAI-1).
Funzioni endocrino-metaboliche
[modifica]Metabolismo delle lipoproteine plasmatiche
[modifica]L'intervento dell'endotelio sul metabolismo delle lipoproteine plasmatiche include il trasferimento delle LDL nel subendotelio e l'attività delle triglicerido-lipasi: lipoproteinlipasi (LPL), lipasi endoteliale (EL) e lipasi epatica (HL) (vedi Lipoproteina - Metabolismo delle lipoproteine plasmatiche). Queste lipasi sono enzimi chiave del metabolismo delle lipoproteine. La loro azione consiste nella idrolisi (scissione per inserimento di una molecola di acqua nel substrato) dei trigliceridi contenuti nei chilomicroni, sintetizzati dalla mucosa intestinale durante il pasto, nelle lipoproteine a densità molto bassa (VLDL), sintetizzate dal fegato, e nelle lipoproteine a densità intermedia (IDL). Tutte queste proteine hanno la funzione di veicolare nel sangue i grassi, principalmente i trigliceridi, che sono insolubili in acqua. Gli acidi grassi liberati dalle lipoproteine plasmatiche possono così attraversare l'endotelio e raggiungere i tessuti.
La LPL è presente sia nei capillari che nelle arterie; è sintetizzata dalle cellule dei tessuti, le quali la secernono negli spazi interstiziali, da dove viene endocitata dalle cellule endoteliali e trasportata sulla loro superficie luminale. Una volta esposta sulla superficie endoteliale, essa si ancora agli eparansolfato-proteoglicani di membrana. La LPL lega le liporoteine plasmatiche e promuove l'idolisi dei loro trigliceridi, determinando la trasformazione dei chilomicroni e delle VLDL nelle particelle rimanenti (IDL), che hanno un più basso contenuto lipidico. In questo processo interviene anche la proteina di membrana GPIHBP1 (glycosylphosphatidylinositol HDL binding protein 1), che fornisce la piattaforma sulla quale vengono in contatto la lipoproteinlipasi e le lipoproteine plasmatiche. La LPL che si trova a livello interstiziale concorre alla patogenesi dell'aterosclerosi (vedi Patobiologia dell'aterosclerosi).
La HL è sintetizzata dagli epatociti ed è esposta sull'endotelio dei sinusoidi epatici, dove svolge azione sovrapponibile alla precedente, con la differenza che i suoi substrati sono i chilomicroni rimanenti, le IDL e le HDL. L'EL è l'unico enzima della famiglia ad essere sintetizzato dalle cellule endoteliali; la sua attività si rivolge soprattutto ai fosfolipidi delle lipoproteine plasmatiche con liberazione degli acidi grassi.
Metabolismo dell'angiotensina
[modifica]L’endotelio ha un ruolo determinante nella produzione dell’ormone angiotensina II (ATII), che rappresenta uno dei più potenti agenti che aumentano la pressione arteriosa: l’ATII è uno dei più potenti vasocostrittori e una delle più potenti sostanze sodio-ritentrici (sostanze che inducono il riassorbimento renale di sodio). Sulla superficie endoteliale è esposto l’enzima convertitore dell’angiotensina (ACE), enzima coinvolto nella regolazione della pressione arteriosa. In particolare l’ACE catalizza la rimozione per idrolisi del dipeptide terminale dell’angiotensina I, fisiologicamente inattiva, formando l’octapeptide angiotensina II, biologicamente attivo. La conversione si verifica per la gran parte quando il sangue passa attraverso i polmoni, ma in grado minore avviene anche nelle altre parti dell’organismo. È stato dimostrato che circa il 100% dei capillari polmonari esprime l'ACE contro il 10-15% di quelli della circolazione sistemica. L'ACE idrolizza anche la bradichinina, un peptide vasodilatatore, inattivandola.
L'ACE è una singola molecola polipeptidica inserita nella membrana plasmatica luminale delle cellule endoteliali. L'enzima possiede pertanto un dominio extracellulare, in cui risiede l'attività enzimatica, un dominio transmembranaceo e uno intracellulare, citoplasmatico. Un altro enzima di membrana, l'ACE secretasi, è in grado di scindere il dominio extracellulare dell'ACE, liberando così l'enzima in circolo.
Tessuto Cordoide
[modifica]Il Tessuto Cordoide è un tessuto di sostegno, a volte erroneamente classificato come tipo particolare di tessuto cartilagineo. Costituisce la corda dorsale (notocorda), presente durante lo sviluppo embrionale in tutti i Cordati; in alcuni vertebrati la corda dorsale può restare anche nell'individuo adulto, in rapporto con lo scarso sviluppo delle vertebre; nei Mammiferi si riduce rimanendo a costituire il nucleo polposo del disco intervertebrale. Nel tessuto cordoide è praticamente assente la sostanza fondamentale; le cellule, una accanto all'altra, sono voluminose e globose e risultano deformate per reciproca compressione; il citoplasma è scarso e confinato alla periferia della cellula assieme al nucleo. Le cellule contengono una notevole quantità di glicogeno (asportato nei comuni preparati istologici) che attira acqua, determinando il caratteristico turgore di queste cellule.
Tessuto Adiposo
[modifica]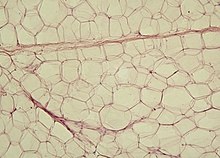
Il Tessuto Adiposo è formato da cellule dette adipociti, ed è diviso in tessuto adiposo bianco e tessuto adiposo bruno.
Tessuto adiposo bianco o giallo
[modifica]Questo sottotipo di tessuto è costituito dalle cellule adipose uniloculari ed è il tessuto adiposo più diffuso nell'organismo umano. Si presenta giallo o biancastro quando è osservato al microscopio ottico.
Struttura
[modifica]Le cellule che lo formano sono grandi (50-100 micron) e molto particolari: il nucleo e tutti gli organelli sono pigiati in un angolino della cellula da una grossa goccia di trigliceridi. Queste cellule si riuniscono in gruppetti (lobuli di grasso) e separati da connettivo lasso. È presente in larga quantità nell'ipoderma e, in misura minore, nel mesentere e nel mediastino. La membrana citoplasmatica dell'adipocita contiene enzima particolare: la lipoproteinlipasi; mentre nel citoplasma ce n'è un altro, il cui funzionamento, è stimolato o inibito da ormoni: si chiama, appunto, lipasi ormone dipendente.
Funzioni
[modifica]Le funzioni del tessuto adiposo bianco o giallo (colore fisiologico) sono solamente :
- funzione meccanica: occupa interstizi, riveste i nervi, i vasi ed i muscoli foderandoli. Riempie alcuni interstizi del midollo osseo. Funge da "cuscinetto" protettivo in parti del corpo diverse in base all'età e al sesso;
- funzione termoisolante (o coibente): il grasso non conduce il calore, per cui non disperde il calore generato dall'organismo;
- funzione di riserva: la membrana citoplasmatica dell'adipocita contiene la lipoproteinlipasi, un enzima che scalza i lipidi dalle loro proteine vettrici (lipoproteine epatiche o chilomicroni enterici) e scinde questi ultimi in glicerina ed acidi grassi; questi ultimi passano la membrana ed entrano nel citoplasma, dove sono riconvertiti in lipidi. La conversione in lipidi può essere anche fatta da glucosio. Inoltre, gli adipociti possiedono anche la lipasi ormone-dipendente, che agisce tagliando i trigliceridi in glicerina ed acidi grassi, su stimolo dell´ormone della crescita, testosterone, glucagone, dell'adrenalina, della tiroxina, della triiodotironina e del neurotrasmettitore noradrenalina. Questo fa sì che i prodotti della lisi fuoriescano dalla cellula e s'attacchino all'albumina ematica per essere portati dove ce n'è bisogno.
Oltre a queste tre, ci sono altre importanti funzioni di questo tessuto:
- è parte integrante della regolazione dell'appetito
- è parte integrante della regolazione del metabolismo
- è coinvolto nelle funzioni della fertilità umana
- regola in misura rilevante la formazione e la differenziazione di cellule ematiche
- è coinvolto nei processi della coagulazione del sangue
- gioca un ruolo centrale in diversi meccanismi di difesa immunitaria aspecifici e specifici, cellulari e umorali.
- in caso di infezioni libera dei mediatori immunitari che attivano e stimolano le difese immunitarie
- pare che in estremi stati di sottopeso (BMI<18 kg/m^2) e di sovrappeso (BMI>42 kg/m^2) possa indurre stati infiammatori cronici.
Il cortisolo e gli androgeni lo fanno accumulare prevalentemente nell'addome e in generale nella parte alta del corpo (biotipo androide), mentre gli estrogeni tendono a distribuirlo soprattutto nella zona glutei, cosce, arti inferiori (biotipo ginoide). Un adulto sano ne ha il 10-15% in peso, altrimenti è sottopeso (se ne ha molto meno), sovrappeso (se ne ha poco più) oppure è affetto da obesità (più o meno grave; secondo la quantità di grasso). È impossibile che cellule di questo tipo muoiano spontaneamente, mentre è possibile che si riduca di molto il loro volume, soprattutto con l'esercizio fisico. D'altro canto recenti ricerche hanno dimostrato come una dieta ricca di grassi idrogenati possa favorire la trasformazione degli adipociti in "adipoblasti" che, riproducendosi, provocherebbero l'ispessimento dello strato adiposo.
Tessuto adiposo bruno
[modifica]
Questo sottotipo di tessuto è costituito dalle cellule adipose multiloculari (al contrario dei normali adipociti non hanno un'unica goccia lipidica ma tante piccole gocce che aumentano la superficie di combustibile esposta al citosol e lo rendono quindi più disponibile per il metabolismo cellulare), è molto scarso nell'uomo adulto e appare brunastro se osservato al microscopio ottico, sia per la presenza massiccia di mitocondri che per l'elevata vascolarizzazione.
Il tessuto adiposo bruno ha esclusivamente la funzione di produrre calore perché i mitocondri delle cellule adipose multiloculari hanno meno ATP sintetasi, l'enzima che catalizza la sintesi dell'ATP, a partire dall'ADP, da fosforo inorganico e dall'energia derivante dalla respirazione cellulare. Posseggono invece una proteina canale (la termogenina) la quale dissipa il gradiente elettrochimico degli ioni idrogeno che il ciclo di krebs normalmente produce a cavallo tra la membrana interna e lo spazio intermembrana. Questa peculiarità fa sì che l'energia prodotta dalla scissione dei trigliceridi non venga utilizzata per la produzione di ATP e venga trasformata in calore.
Il grasso bruno è ben rappresentato nei neonati di molte specie (nella specie umana soprattutto a livello della nuca, del collo e delle scapole). Negli adulti è abbondante invece quasi esclusivamente nelle specie che vanno in letargo, mentre negli adulti di altre specie, compresa quella umana, esso è scarsamente presente (l'esistenza di due diverse tipologie di lipoma, cioè di neoplasie del tessuto adiposo, mostra però la permanenza di due diverse tipologie di tessuto adiposo anche nell'individuo adulto).

