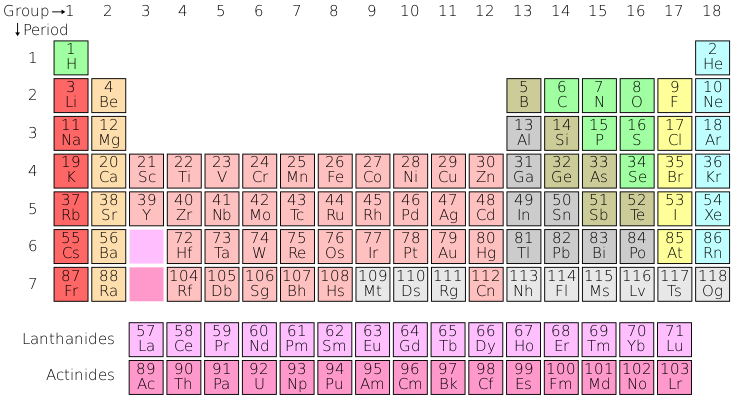
Tavola periodica degli elementi
La tavola periodica, inventata dal chimico Dimitrij Mendeleev, fa parte delle conoscenze base dei chimici, dai dilettanti ai professionisti. Essa raggruppa gli elementi secondo un preciso ordine, che tiene conto della loro configurazione elettronica. La tavola è divisa in periodi e gruppi.
PERIODI
I periodi dividono la tavola in orizzontale; prendiamo in esempio il 2° periodo: Litio, Berillio, Boro, Carbonio, Azoto, Ossigeno, Fluoro e Neon e osserviamo questo: il Litio ha numero atomico (Z) di 3; il Berillio Z=4, il Boro Z=5, il Carbonio Z=6, l'Azoto Z=7, e così via; man mano che andiamo avanti Z aumenta di uno per elemento; questo è il criterio del periodo; in esso vi sono raggruppati gli elementi in ordine crescente, aumentando di uno per ogni passaggio; i periodi sono 7 in tutto; di solito vi sono 18 elementi per periodo, tranne nel primo, in cui ce ne sono 2, nel secondo e nel terzo, in cui ce ne sono 8.
GRUPPI
I gruppi, invece, la dividono in verticale, e sono diciotto; per ogni gruppo, gli elementi in esso classificati hanno lo stesso numero di elettroni nell'ultimo livello energetico (livello di valenza); prendiamo in esempio il primo gruppo; gli elementi in esso contenuti sono: Idrogeno, Litio, Sodio, Potassio, Rubidio, Cesio, Francio; ognuno di essi ha un elettrone nell'ultimo livello; ogni gruppo ha sette elementi.
Esercizi per capire la tavola periodica
[modifica]