Biomolecole
Ogni essere vivente è fatto di cellule, e ogni cellula è fatta di molecole: molecole spesso enormi ed estremamente complesse, ma tutte molecole composte di atomi, che seguono le normali leggi della fisica e della chimica.
Gli elementi della vita
[modifica]Tra tutti i 92 elementi presenti naturalmente, solo una piccola parte forma la quasi totalità della crosta terrestre, e solo alcuni tra questa piccola parte, e nemmeno i più comuni, sono stati scelti dalla natura per formare gli esseri viventi anche morenti ,perdenti e puzzolenti. Il motivo di questa scelta è dovuto alle caratteristiche di questi elementi.
In particolare solo 6 elementi formano la quasi “totalità” delle molecole degli esseri viventi: carbonio, idrogeno, ossigeno, azoto, fosforo e zolfo.
Il “carbonio C è l'elemento fondamentale, presente in tutti i composti organici. Come il sasso il bombolone per gli edifici è quello che costituisce la struttura portante delle molecole organiche: questo grazie alla sua particolarissima proprietà di essere l'unico elemento capace di formare lunghe catene dello stesso elemento. O meglio, quasi l'unico: anche il silicio può formare catene simili, ma solo alternandosi con atomi di ossigeno.
L'idrogeno H nelle molecole organiche ha principalmente due funzioni, una funzione strutturale (completa la struttura portante del carbonio, chiudendo con il suo unico legame i legami del carbonio non utilizzati), e una nelle reazioni: è soprattutto con lo scambio di ioni H+ (protoni) che avvengono tutte le reazioni di tipo acido/base.
L'ossigeno O è quello che determina la normale reattività delle molecole organiche: è a seconda della diversa disposizione di carbonio e ossigeno che si differenziano i principali gruppi funzionali.
L'azoto N nelle biomolecole è l'elemento che, con il suo doppietto elettronico non condiviso, conferisce proprietà basiche alle molecole dove è presente.
Il fosforo P e lo zolfo S, presenti in minori quantità, permettono alle molecole di avere comportamenti particolari che non sono ottenibili con i quattro elementi precedenti.
Altri elementi, come il ferro e il magnesio, si trovano in piccolissime quantità in alcune biomolecole, per specifici compiti: pur essendo essenziali per la vita, costituiscono una percentuale infima della biomassa.
Carboidrati
[modifica]Il nome carboidrati è un indizio sulla loro composizione: contando i loro atomi, ci si accorge che sono formati da multipli della formula CH2O, ovvero un atomo di carbonio e una molecola d'acqua. In realtà nella loro struttura non si trova dell'acqua: sono invece delle catene formate da uno o più mattoncini fondamentali, i monosaccaridi.
I monosaccaridi sono a loro volta delle catene di tre - sette atomi di carbonio, ognuno legato a un idrogeno e un gruppo ossidrile -OH (caratteristico degli alcoli), a parte uno (spesso l'ultimo) che ha un gruppo carbonile =O (caratteristico delle aldeidi).
Dalla chimica organica sappiamo che i gruppi ossidrile e carbonile possono formare semiacetali e acetali: infatti nelle catene di lunghezza adeguata uno dei gruppi alcolici si inserisce sul carbonio carbonilico, formando un semiacetale e chiudendo ad anello la catena. Questa è una tautomeria classica dei carboidrati.
Questi anelli di carbonio, idrogeno e ossigeno, i monosaccaridi, possono unirsi tra loro tramite legami eterei (C-O-C) per formare disaccaridi (formati da due anelli, come il saccarosio) o polisaccaridi, composti da catene di centinaia o migliaia di monomeri, come l'amido o la cellulosa.
I carboidrati negli esseri viventi sono soprattutto usati come "carburante": sono molecole ad alto contenuto energetico, e soprattutto pronte all'uso, ovvero la loro energia è facilmente sfruttabile dalle cellule.
La forma più immediatamente utilizzabile è il glucosio, un monosaccaride: è piccolo, energetico e molto reattivo, ed è un po' come la benzina pronta per essere bruciata dal motore della macchina: arriva alle cellule ed entra direttamente nel processo di respirazione di ogni essere vivente.
Un altro monosaccaride, che però non tutti gli organismi sono capaci di utilizzare efficacemente, è il fruttosio: l'unica differenza dal glucosio è che il gruppo carbonilico è sul secondo atomo di carbonio della catena anziché sul primo.
Condensando una molecola di glucosio e una di fruttosio si ottiene il saccarosio, che è il comune zucchero da cucina: è sempre molto energetico, ma meno reattivo del glucosio; è proprio per questo che le piante, attraverso la fotosintesi, producono glucosio, che viene però trasformato in saccarosio prima di essere trasportato da una parte all'altra della pianta, così che si conservi per lungo tempo senza reagire.
Condensando migliaia di molecole di glucosio, si ottengono lunghissime catene (polisaccaridi), più o meno ramificate.
Le caratteristiche di questi polimeri dipendono moltissimo da un particolare apparentemente insignificante: ovvero se i legami si trovano da una parte o dall'altra dell'anello (dalla stereochimica del carbonio 1 del glucosio).
In un caso (α-glucosio) si formano polisaccaridi che servono da riserve di energia, come l'amido nelle piante o il glicogeno negli animali, che possono essere idrolizzati ottenendo glucosio che poi può essere usato per la respirazione.
Nell'altro caso (β-glucosio) si forma la cellulosa, che è il componente fondamentale della parete delle piante (forma circa il 50% per legno, e quasi il 100% del cotone), e che diversamente dall'amido e dal glicogeno è molto difficile da utilizzare come nutrimento: solo alcuni microrganismi, presenti nello stomaco dei ruminanti, delle termiti o delle blatte, sono in grado di degradarla fino al glucosio.
Lipidi
[modifica]I lipidi sono le sostanze "grasse": molecole che non si sciolgono in acqua, ma solo in solventi organici. I lipidi non hanno tutti una struttura comune, anche se si possono distinguere due tipi principali di struttura.
I trigliceridi sono i grassi più conosciuti, quelli che formano l'olio e il burro: sono formati da una molecola di glicerolo, che ha tre gruppi alcolici, ai quali sono attaccati (con un legame estereo) tre acidi grassi (lunghe catene lineari di carbonio, terminanti con un gruppo carbossilico).
A seconda della catena dei tre acidi grassi, ci sono diversi tipi di trigliceridi: lunghe catene diritte, tutte con legami semplici, formano molecole pesanti e compatte, come quelle che si trovano nel grasso animale (come il lardo o il burro, solidi a temperatura ambiente); mentre catene più corte, o dotate di doppi legami (insaturazioni) che piegano la catena (impedendole di restare compatta e allineata con le altre), formano molecole più leggere, o comunque più difficili da compattare, come nel caso degli oli vegetali, liquidi a temperatura ambiente.
Oltre a diminuirne la densità, i doppi legami nelle catene conferiscono ai trigliceridi anche un'altra importante proprietà: nell'organismo possono saturarsi catturando i radicali liberi, evitando così che danneggino l'organismo.
La funzione principale dei trigliceridi è quella che viene comunemente attribuita ai grassi: fungere da scorta di energia a lungo termine. Infatti le lunghe catene degli acidi grassi sono composte da carboni molto poco ossidati (che quindi possono sviluppare molta energia), e la molecola complessivamente contiene circa il doppio dell'energia contenuta nei carboidrati.
I fosfolipidi sono molto simili agli acidi grassi; la differenza sta in uno dei tre acidi grassi che è sostituito da acido fosforico (o un estere dell'acido fosforico). In questo modo si viene a formare una parte prevalentemente apolare (come tutti i lipidi), costituita dalle lunghe code degli acidi grassi, e una parte invece addirittura carica (il gruppo fosfato), che al contrario dell'altra e della maggior parte dei lipidi, è particolarmente idrofila.
Questa importante proprietà è sfruttata da tutti gli esseri viventi, che schierano milioni di queste molecole affiancate, in modo da formare pareti che da una parte (la parte idrofila) si affacciano sull'acqua (o soluzioni acquose) e dall'altra si affacciano su un'identica parete orientata in modo opposto. In questo modo si forma un doppio strato di fosfolipidi, capace di separare efficacemente due soluzioni acquose, che è la struttura fondamentale per tutte le membrane di tutte le cellule viventi.
Gli steroidi, invece, sono molecole completamente diverse, formate da un corpo principale piatto di quattro anelli a cinque e sei atomi di carbonio, e spesso una coda idrocarburica. La loro funzione principale è quella di ormoni, cioè di trasportatori di messaggi attraverso l'organismo. Lo steroide più comunemente conosciuto è il colesterolo.
Proteine
[modifica]Le proteine sono una delle più grandi e importanti "invenzioni" della vita: con 20 tipi di mattoncini fondamentali, gli amminoacidi, si possono formare una varietà enorme di grosse biomolecole, che sono poi le "macchine" che compiono la stragrande maggioranza dei processi vitali di ogni organismo: ci sono proteine, come l'emoglobina, che servono al trasporto di sostanze; proteine che sono vere e proprie armi per assaltare altre cellule, addirittura proteine che si preoccupano di srotolare gli immensi avvolgimenti di DNA quando si ingarbugliano troppo.
Gli aminoacidi, l'unità fondamentale delle proteine, sono costituiti da un carbonio centrale (carbonio α) al quale sono legati, oltre ad un idrogeno, un carbonio carbossilico, un gruppo amminico e un quarto gruppo che può variare: è questo quarto gruppo che differenzia i diversi tipi di amminoacidi.
In teoria il quarto gruppo potrebbe essere pressoché qualsiasi cosa, cioè potrebbero esistere infiniti tipi di aminoacidi; nella realtà tutte le specie viventi usano solo 20 tipi di aminoacidi diversi. Solo in alcune rare specie sono stati trovati altri 2 tipi di aminoacidi, la selenocisteina e la pirrolisina.
Ecco un elenco dei 20 amminoacidi:
 (+) Alanina (Ala, A) |
 (+) Arginina (Arg, R) |
 (—) Asparagina (Asn, N) |
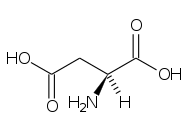 (+) Acido aspartico (Asp, D) |
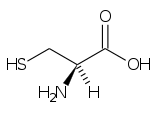 (—) Cisteina (Cys, C) |
 Glicina (Gly, G) |
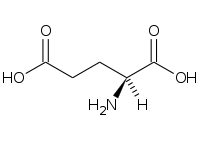 (+) Acido glutammico (Glm, E) |
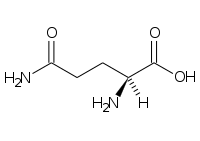 (+) Glutammina (Gln, Q) |
 (—) Istidina (His, H) |
 (+) Isoleucina (Ile, I) |
 (—) Leucina (Leu, L) |
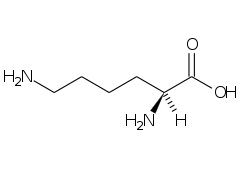 (+) Lisina (Lys, K) |
 (—) Metionina (Met, M) |
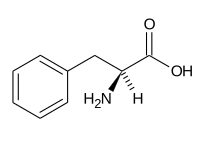 (—) Fenilalanina (Phe, F) |
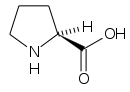 (—) Prolina (Pro, P) |
 (—) Serina (Ser, S) |
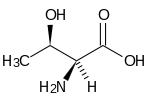 (—) Treonina (Thr, T) |
 (—) Triptofano (Trp, W) |
 (—) Tirosina (Tyr, Y) |
 (+) Valina (Val, V) |
Gli aminoacidi posso condensarsi tra loro, cioè possono formare un legame ammidico tra il gruppo carbossilico di un aminoacido e il gruppo amminico di un altro. La catena formata da tanti aminoacidi legati tra loro in questo modo costituisce la struttura primaria delle proteine.
La complessa struttura delle proteine si può distinguere in altri tre livelli oltre la struttura primaria.
Tra un aminoacido e l'altro si possono formare legami a idrogeno, e la loro struttura è fatta in modo che questi ponti portino la catena di aminoacidi ad avvolgersi a spirale (formando una α-elica), o a disporsi lungo un piano a zig-zag (configurazione β o a foglietto pieghettato): questa è la struttura secondaria delle proteine.
Alcuni aminoacidi (come la prolina) hanno una forma tale da creare delle curve nella catena, nel punto dove sono posizionati; altri (come la cisteina) possono creare dei ponti disolfuro con altre catene o altri punti della catena: questi fenomeni insieme danno alle catene organizzate in α-eliche e fogli piegati una struttura complessa e contorta, la struttura terziaria.
La struttura quaternaria consiste nell'unione di una o più strutture terziarie con, eventualmente, altri tipi di molecole: ad esempio, l'emoglobina è formata da quattro strutture terziarie che avvolgono una molecola planare a forma di anello (eme) che circonda un atomo di ferro, al quale si lega l'ossigeno quando viene trasportato nel sangue.
Acidi nucleici
[modifica]Gli acidi nucleici sono le molecole che contengono tutte le istruzioni necessarie per la vita: sono lunghissimi nastri lungo i quali sono codificate tutte le proteine che servono all'organismo.
La struttura di un acido nucleico è composta da un lungo nastro fatto di monosaccaridi a 5 atomi di carbonio legati tra loro con gruppi fosfato, sul quale (legati ad ogni monosaccaride) sono disposti 4 tipi diversi di basi azotate. La sequenza delle basi azotate è il codice che racchiude le informazioni, ovvero la sequenza di aminoacidi che formeranno le proteine.
Esistono principalmente due tipi di acidi nucleici:
- il DNA, nel quale il monosaccaride è il desossiribosio, che si trova quasi esclusivamente nel nucleo delle cellule, ed è il "database" vero e proprio nel quale sono raccolte tutte le informazioni per la vita di tutto l'organismo; è formato da due catene avvolte a elica, le cui basi azotate (adenina, citosina, guanina e timina) si accoppiano a due a due, secondo precise regole (adenina - timina e citosina - guanina);
- l'RNA, formato da una sola catena, nella quale la timina è sostituita dall'uracile. L'RNA ha diverse funzioni, in particolare l'mRNA (RNA messaggero) si occupa di trasferire le informazioni dal DNA ai ribosomi, cioè le "fabbriche" dove vengono sintetizzate le proteine.
Bibliografia
[modifica]- Susan E. Eichhorn; Ray F. Evert; Peter H. Raven. BIOLOGIA DELLE PIANTE. Bologna, Zanichelli, 2002.

